ADC原液工艺开发
ADC创新的崛起正在重塑靶向治疗的发展,全球ADC市场预计到2030年将达到685亿美元,年均增长率超过30%*。这一快速扩展推动了对强大、可扩展且具有成本效益的ADC工艺开发的需求。
然而,每一个成功的ADC背后,都有一个复杂的ADC 原液开发过程,其中包括关键环节如载荷-连接子合成, 抗体生产和 ADC 偶联。这些要素构成了高质量、高效率ADC工艺开发的基础。
在皓元医药,我们将先进的化学合成、生物制剂专业知识和创新的连接技术相结合,基于“质量源于设计”(QbD)驱动的平台,提供更快捷、更安全、更具成本效益的ADC原液工艺开发解决方案,以应对当今竞争激烈的市场环境。
*Source: Frost & Sullivan 2025 China Pharmaceutical CDMO Industry Insight Blue Book

一站式ADC CDMO服务
皓元医药提供从载荷-连接子到ADC原液&制剂的全方位服务,实现高效的规模化生产和无缝的技术转移, 有效降低管理和过渡成本。

丰富的项目经验与丰富库存
我们已成功交付超过 170 个 ADC 项目,包括 70 + CMC 项目、5 个 BLA 项目和 1 个商业化项目,16 个与 ADC 药物相关的小分子产品在美国 FDA 注册了 DMF。

卓越的专家团队
我们拥有超过600 名科学家的团队,从研发到商业化生产提供全面支持,确保为您的 ADC 管线提供高质量、可扩展的解决方案。
我们的服务
与我们合作,开展前沿、高效的ADC原液工艺开发,从药物载荷-连接子合成到ADC偶联。我们提供定制化ADC工艺开发解决方案,简化复杂挑战,降低风险,加快上市进程——让您的创新更快实现。
我们的服务项目包括
ADC载荷-连接子合成
- 工艺参数优化
- 不稳定中间体稳定性研究
- 纯化方法研究
- 杂质控制策略研究
- 工艺表征与验证
抗体工艺开发
- 快速工艺开发
- 表达与纯化工艺优化
- 裸抗冻融实验
- 中间品稳定性
- 裸抗工艺表征
- 放大生产
偶联工艺开发
- 多类型偶联技术:半胱氨酸偶联 (-SH)、赖氨酸偶联 (-NH2)、N-糖偶联以及酶偶联等
- 双Payload偶联
- 偶联工艺开发及确认
- 偶联中间体稳定性研究
- DAR 2.0/4.0/8.0±0.3精准控制
- 游离药物控制
- 可放大的偶联工艺
- 原液冻融实验
- 原液工艺表征与验证
- GMP技术无缝转移
合作优势
一站式服务
通过模块化开发,提供从载荷-连接子, 抗体到ADC原液的无缝解决方案,13个月从 DNA-IND,优化效率和可扩展性, 确保您的项目按时达成目标
灵活运行和成本效益
通过灵活执行和快速周转,配合一站式服务无缝衔接,有效降低管理成本和切换成本
精准控制
可定制 DAR 分布(2.0/4.0/8.0±0.3),单体纯度>98%(SEC-HPLC验证),确保高质量和可重复性
多样化偶联技术
基于非定点与定点偶联技术,支持半胱氨酸偶联、赖氨酸偶联、N-糖偶联以及酶偶联等工艺, 为您的需求量身定制解决方案,如SEC、DAR、游离小分子的质量控制等
不同规模的偶联反应釜
配备50L、100L、200L与500L工艺开发偶联反应釜,满足不同偶联规模需求,并验证不同规模放大稳定性
绿色化学
获得 EcoVadis 银牌认证,推动绿色化学实践,提高效率和可持续性
我们的基地
研发基地
生产基地
案例研究
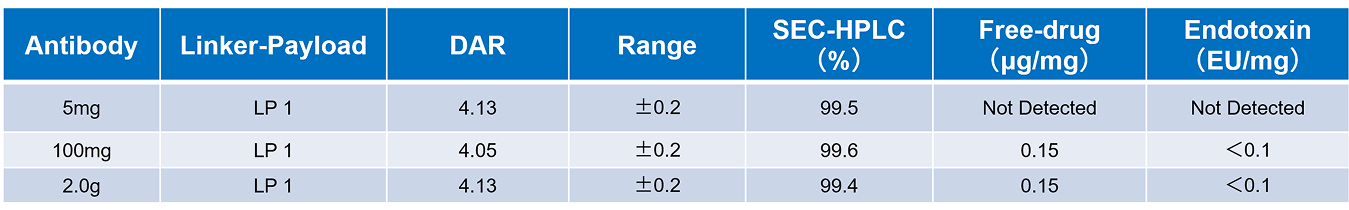
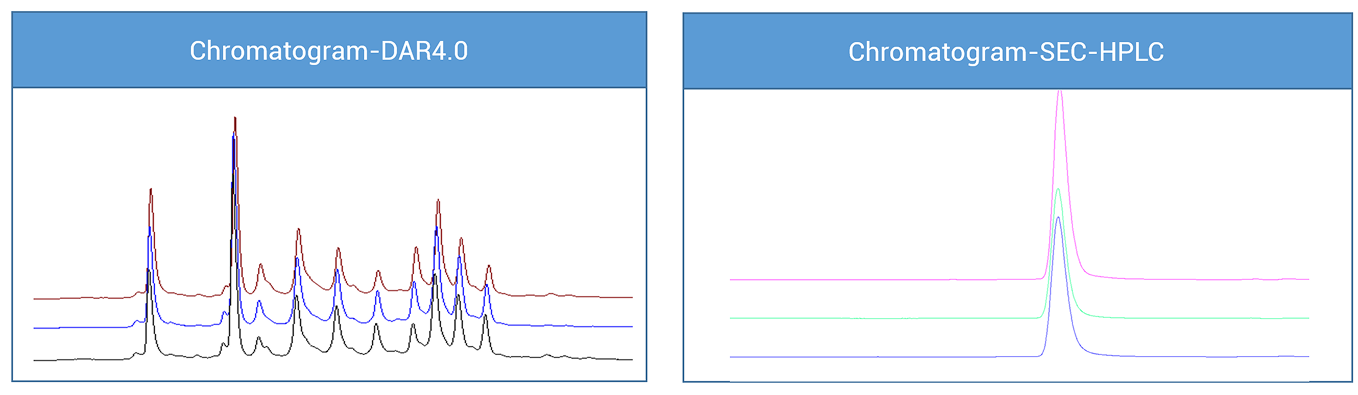
在进行双抗偶联DAR4的工艺开发过程中,研究人员发现,随着反应规模的扩大,从20mg、300mg逐步放大至3.0g的过程中, 偶联产物的稳定性表现出了良好的可控性。但初期分析中仍存在小分子残留和内毒素水平波动的风险。为了进一步提高产品质量,并确保在不同工艺条件下的稳定性,团队采用了快速方法优化 策略。特别是在小分子残留和内毒素水平的控制方面,通过优化偶联反应条件和净化流程,最终成功实现了:
· 偶联后SEC-HPLC纯度:大于99%
· 小分子残留:低于0.11μg/mg
· 内毒素含量:低于0.1EU/mg
常见问题解答
这是一个关于ADC生产流程的关键问题。简单来说,ADC工艺开发是一个总称,它涵盖了从抗体-载荷-连接子到最终成品制剂的完整开发过程。它可以明确地分为以下两个核心阶段:
1. ADC原液工艺开发
· 关注点: 此阶段专注于生产ADC的活性药物成分,即未进行最终制剂加工的“裸药”。· 核心内容: 主要包括抗体-药物偶联反应本身的工艺开发与优化。
2. ADC制剂开发
· 关注点: 此阶段专注于将上述步骤生产出的ADC原液转化为可供临床使用的最终药品。· 核心内容: 主要围绕保证最终剂型的稳定性、安全性和适用性。
因此,ADC工艺开发完整地定义了如何从起始物料生产出最终药品的整个技术路径
我们在双特异性抗体及双Payload领域均有丰富的项目经验。目前,我们正在推进一个处于临床II期的双特异性抗体项目。同时,我们已完成双Payload的技术验证及早期样品制备,并持续为PCC阶段提供双特异性抗体样品制备服务,已积累6个双特异性抗体ADC项目的经验。我们的研发与生产团队大多数成员均具备双特异性抗体相关背景,能够为不同阶段的项目提供专业支持。
马来酰亚胺与巯基生成的硫醚键在存在外源性巯基(血清白蛋白上的半胱氨酸和GSH)的情况下,可能发生逆迈克尔加成反应,导致不稳定。这种不稳定性可能会影响药物在循环中的稳定性,增加脱靶毒性,并降低抗体偶联药物(ADCs)的疗效。解决措施:水解开环或改造PL增加PEG及其他改造。









